Adesea, auzim despre osmoză în contextul unor noi tehnologii precum filtrarea și purificarea apei, de exemplu. Reclamele fac procesul să pară ceva nou și uimitor; un stimulent de încredere garantat.
Cu siguranță inspiră uimire, nu atât pentru proces, cât pentru rezultate. Cu toate acestea, nu este o descoperire nouă; lumea noastră naturală și chiar propriile noastre corpuri s-au susținut prin osmoză încă de la începuturile timpului.
În mod clar, osmoza este un proces important în toate științele și, în special, în biologie. Așadar, să începem cu o imagine de ansamblu asupra osmozei și să ne focusăm atenția asupra a ceea ce trebuie să știi despre osmoză pentru recapitularea de bacalaureat, și să încheiem lămurind diferența dintre difuziune și osmoză.
| Aspect | Informații |
|---|---|
| Relația cu difuziunea | Osmoza este similară cu difuziunea, dar se deosebește prin prezența unei bariere semipermeabile |
| Rol biologic | Osmoza are un rol vital în funcțiile biologice: apa intră și iese din celule prin osmoză |
| Factori principali | Osmoza este influențată de gradientul de concentrație și de presiunea osmotică |
| Funcție principală | Osmoza tinde să egalizeze concentrațiile de solut de o parte și de alta a unei membrane semipermeabile, prin deplasarea apei. |

Ce este osmoza?
În termeni generali, osmoza este acțiunea de egalizare a concentrațiilor de soluți de ambele părți ale unei bariere semipermeabile.
Dacă o parte are o concentrație ridicată de soluți, trebuie să existe mai puțină apă prezentă. Dacă, pe cealaltă parte a barierei semipermeabile, există o concentrație mai scăzută de soluți - deci un potențial mai mare pentru apă, moleculele de apă vor trece bariera pentru a face concentrația de soluți egală pe ambele părți.

Ține minte că osmoza este un proces folosit pe scară largă în producție și în alte aspecte ale vieții noastre de zi cu zi; este, de asemenea, un proces frecvent utilizat în studiile și aplicațiile chimice. Adesea aceste procese osmotice folosesc solvenți și soluți - de aici și folosirea acelor cuvinte în descrierea generală de mai sus.
În biologie, osmoza se referă la mișcarea netă a moleculelor de apă prin membranele celulare.
Ne vom concentra asupra osmozei în biologie imediat; deocamdată, să continuăm cu privirea noastră generală asupra osmozei; și anume, vocabularul specific acestui fenomen.
- presiune osmotică
- gradient osmotic
- presiune de turgescență
- hipotonie
- izotonic
- hiperton
- plasmoliză
- flacid
- turgid
Cu acest vocabular stabilit, înainte de a trece la structura celulelor vegetale și animale care permit osmoza, să ne uităm la câțiva factori care pot afecta procesul.
Factorii care afectează osmoza
Doi factori principali afectează procesul osmotic: gradientul de concentrație - numit și gradient osmotic, și presiunea osmotică. Am dat o scurtă definiție pentru ambele în segmentul anterior; acum, să vorbim despre ele mai detaliat.
Celulele vegetale pot „exploda” sau se pot ofili doar din cauza diferențelor de presiune osmotică – dacă sunt puse în apă foarte pură, absorb atât de multă apă încât presiunea internă crește enorm, iar fără peretele celular, celula n-ar supraviețui.
Gradientul de concentrație
Gradientul de concentrație se referă la concentrația particulelor dizolvate într-o soluție; în special, diferența dintre procentele de concentrație. Această condiție există atunci când există o concentrație mai mare de soluți pe o parte a unei membrane semipermeabile decât pe cealaltă.
Imaginează-ți că tocmai ai adăugat un pic de sare într-un pahar cu apă. Punctul în care ai introdus sarea are un gradient de concentrație mai ridicat decât în altă parte în apă și, pe măsură ce se scufundă în fund și se acumulează, acolo este concentrația cea mai mare. Pe măsură ce amesteci apoi sarea în apă, acele molecule se dispersează, distribuind în cele din urmă sarea uniform în întreaga apă.
În acel moment, se spune că soluția a atins echilibrul.
Celulele folosesc gradienții de concentrație pentru a muta o substanță în sau în afara celulelor lor. Energia stocată inerentă gradienților de concentrație este folosită în acest scop.
Poate cel mai evident exemplu de astfel de utilizare are loc în timpul uneia dintre funcțiile noastre cele mai vitale și fundamentale: respirația. Desigur, este o instanță a unui gaz care reflectă un gradient de concentrație, dar poate servi bine pentru a ilustra principiul.
Oxigenul urmează regulile gradienților de concentrație, la fel cum o fac și soluții. Și el difuzează spre zone de concentrație scăzută din zone de concentrație ridicată. Așa se întâmplă că, în timpul trecerii prin plămânii noștri, globulele noastre roșii câștigă oxigen. Mai târziu, pe măsură ce aceste celule circulă prin corpul nostru, ele își pierd conținutul de oxigen; acel gaz difuzează din nou dintr-o zonă de concentrație ridicată (celulele) spre zone cu concentrație scăzută - organele și țesuturile noastre.
Găsește profesori de biologie aici, pe Superprof.

Presiunea osmotică
Pur și simplu, presiunea osmotică reprezintă cât de tare trebuie să împingă apa pentru a trece printr-o barieră semipermeabilă. Această presiune este determinată de concentrația de solut; apa va munci mai mult pentru a accesa o zonă cu o concentrație mai mare de solut.
Desigur, apa nu are voință independentă sau cunoștință despre gradienți de solut; ea pur și simplu se supune legilor naturii care dictează distribuirea aleatorie a materiei.
Ecuația folosită pentru a calcula presiunea osmotică este π = MRT
Acesta este, într-adevăr, simbolul pentru Pi, dar în această ecuație nu reprezintă acea valoare. A fost adoptat prin consens; chimiștii sunt toți de acord că servește bine pentru a reprezenta presiunea osmotică. Rezolvarea pentru π, în acest caz, este la fel ca rezolvarea pentru X în orice altă ecuație algebrică.
Pe cealaltă parte a semnului egal, găsim M (concentrația molară), R (constanta gazului ideal) și T (temperatura [Kelvin]). S-ar putea să nu fii nevoit să faci niciun calcul al presiunii osmotice, dar ai nevoie de cel puțin un exemplu care ilustrează perfect conceptul.
Pentru asta, trebuie să știm puțin despre biologia celulară…

Osmoza în biologie
Ai fost vreodată în vacanță și, la întoarcere, ai găsit plantele tale ofilite? Dar apoi, după ce le-ai dat apă, și-au revenit… aceasta este presiunea osmotică la lucru.
Plantele folosesc presiunea osmotică pentru a-și menține forma; apa „umflă” celulele și le oferă suficient spațiu pentru a funcționa corespunzător. O plantă bine udată, cu frunze verzi vibrante și tulpini pline este izotonică; una care se ofilește este hipertonică - apa s-a mutat din celule și concentrația lor de soluți este acum prea mare.
Când te deshidratezi, celulele din corpul tău suferă același proces: moleculele de apă din mușchi și alte organe se transferă în celulele tale sangvine prin osmoză deoarece acestea sunt hipertonice. Acest lucru lasă o concentrație ridicată de soluți în acele celule, o condiție care ar putea deranja funcția lor.
Ar fi de ajutor să știm funcția structurilor celulare pentru a înțelege pe deplin acel concept, nu-i așa?
Spre deosebire de udarea generoasă a plantelor, nu putem pur și simplu să turnăm găleți de apă pe gât și să sperăm la rezultate instantanee; efectele ar putea fi pur și simplu periculoase. Este nevoie de rehidratare lentă pentru a da timp celulelor noastre să se adapteze la presiunea osmotică.
Găsește un tutore de biologie online aici, pe Superprof.
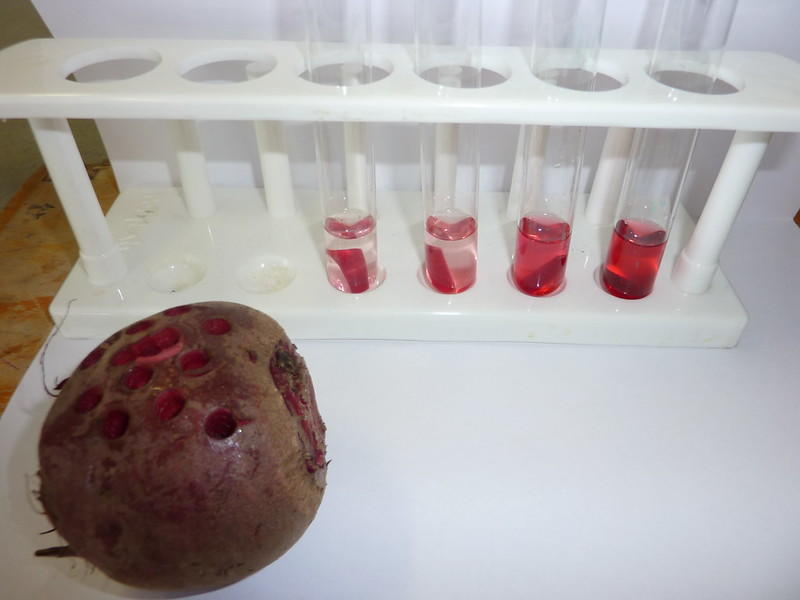
Experimentul cu cartoful pentru osmoza
Feliile (sau cilindrii) de cartof sau sfeclă în grade diferite de apă sărată sau zaharată fac un experiment distractiv care demonstrează efectele osmozei.
Pentru acest experiment, vei avea nevoie de mai multe eprubete - una cu apă simplă și celelalte, cu procente din ce în ce mai mari de sare sau zahăr. Eprubeta cu apă simplă servește ca martor (control); celelalte demonstrează viteza apei care iese din cilindrul de cartof sau sfeclă.
Cu cât concentrația de sare sau zahăr este mai mare, cu atât mai repede proba de cartof se va „deumfla”. În curând, vei vedea cilindrii tăi de cartof micșorându-se și, după ce îi scoți din eprubete și îi cântărești, vei descoperi că și greutatea lor a scăzut.
Pentru a realiza acest experiment, va trebui să tai fâșii dintr-un cartof și să le usuci. Pregătește-ți eprubetele, notând concentrația de solut ca procent pe fiecare. De asemenea, este o idee bună să pregătești un tabel pentru a înregistra observațiile.
Lasă-ți fâșiile de cartof sau sfeclă să stea în soluțiile lor timp de 20 de minute, apoi, scoate-le, usucă-le și ia-le greutatea. Care au fost rezultatele tale?
Nu este suficient să faci acest proces o singură dată; pentru rezultate cu adevărat științifice, ar trebui să repeți experimentul pentru a vedea dacă obții aproximativ aceleași rezultate. Abia atunci ai stabilit dovada că apa din celulele de cartof s-a mutat în soluție pentru a egaliza balanța de soluți.
Un meditator de biologie poate oferi feedback continuu și încurajare pentru a menține motivația elevilor.
Diferența dintre difuziune și osmoza
Răsfoind manualul de biologie pentru a recapitula materia de bac, poate ai observat că „difuziunea” și „osmoza” sunt folosite aparent la întâmplare. Dacă asta te-a lăsat gânditor, nu ești singur: mulți nu înțeleg chiar diferența dintre difuzie și osmoză.
În principiu, ele reprezintă același lucru: egalizarea concentrației de soluți. Cu toate acestea, în timp ce difuziunea se poate întâmpla în orice condiții, osmoza are loc doar atunci când există o barieră semipermeabilă de traversat.
Pe lângă prezența unei astfel de membrane, diferența majoră dintre difuziune și osmoză este că, în aceasta din urmă, doar apa traversează membrana. În difuziune, atât particulele de solut, cât și cele de solvent se mișcă pentru a egaliza gradientul de concentrație.
Ține minte că, în alte domenii și alte științe, osmoza are loc folosind alți soluți. Cu toate acestea, în biologie, solutul în cauză este doar apa.
În toate cazurile, osmoza poate fi considerată un tip special de difuziune, care necesită prezența unei membrane semipermeabile pe care doar solutul o poate traversa.
Mai sunt multe de spus despre difuziune: scopul și utilitatea ei în organisme, cum funcționează în plante și animale și care factori afectează difuzia.
Viața există deoarece moleculele respectă reguli simple, iar din aceste reguli apare echilibrul.
Jacques Monod
Rezumă cu AI:














